近日,国家标准化委员会发布了GB/T 19002-2018《质量管理体系 GB T 19001-2016应用指南》,该标准按照ISO/TC176/ SC2质量体系主席Nigel H. Croft评价:“为未来 25 年的质量管理标准做好准备”。

GMP给出了制药质量管理的内容要求,而GB T 19001/ISO 9001则给出了质量管理的方法。解读如下:
给出了基于PDCA(Plan-Do-Chcek-Act)循环的质量管理方法:
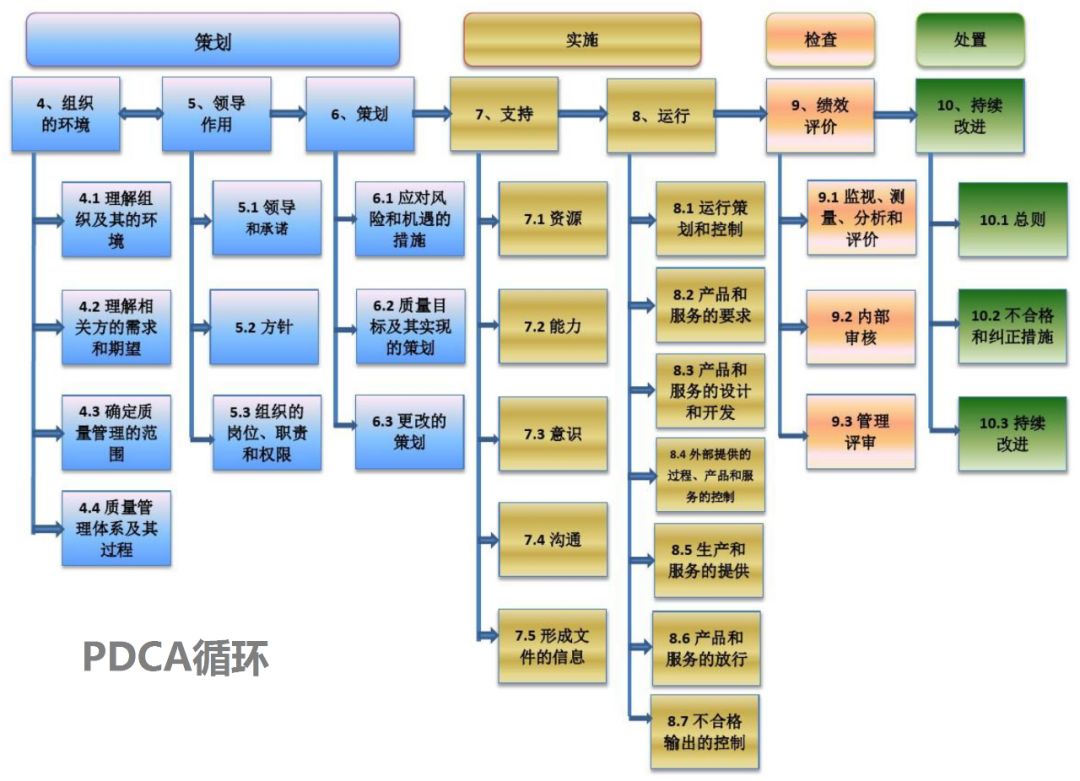
标准取消了质量手册等强制性文件的要求
该标准与GMP条款相比更加强调高级管理层的作用,高级管理层包括诸如首席执行官、总裁、总经理、董事长、董事会、执行董事、执行合伙人、单一所有人、合伙人和髙级管理人员等。
高级管理者应通过以下方面,证实其对质量管理体系的领导作用和承诺:
a)对质量管理体系的有效性负责;
b)确保制定质量管理体系的质量方针和质量目标,并与组织环境相适应,与战略方向相一致;
c)确保质量管理体系要求融入组织的业务过程;
d)促进使用过程方法和基于风险的思维;
e)确保质量管理体系所需的资源是可获得的;
f)沟通有效的质量管理和符合质量管理体系要求的重要性;
g)确保质量管理体系实现预期结果;
h)促使人员积极参与、指导和支持他们为质量管理体系的有效性作出贡献;
i)推动改进;
j)支持其他相关管理者在其职责范围内发挥领导作用。
最高管理者应制定、实施和保持质量方针,质量方针应:
a)适应组织的宗旨和环境并支持其战略方向;
b)为建立质量目标提供框架;
c)包括满足适用要求的承诺;
d)包括持续改进质量管理体系的承诺。
关于质量方针的要求,应:
a)可获取并保持成文信息
b)在组织内得到沟通、理解和应用;
c)适宜时,可为有关相关方所获取。
关于质量体系的范围,要求应基于以下内容确定体系的范围:
内部因素(如组织绩效、资源、人员、文化、战略等);
外部因素(如经济、社会、政治、技术、市场等)
相关方(如监管方和顾客)的要求;
组织提供的产品和服务。
在确定体系范围时,组织还应通过考虑以下因素,确定质量管理体系的边界:
——组织的基础设施;
——组织的不同场所和活动;
——商业政策和战略;
——组织集中控制或由外部提供的职能、活动、过程、产品和服务。
关于质量目标的制定,要求如下:
a)与质量方针保持一致;
b)可测量;
c)考虑适用的要求;
d)与产品和服务合格以及增强顾客满意相关;
e)予以监视;
f)予以沟通;
g)适时更新。
实现质量目标时,应确定:
a)要做什么;
b)需要什么资源;
c)由谁负责;
d)何时完成;
e)如何评价结果。
该指南与GMP的另一个不同是,给出了质量管理评审手段
管理评审输入
策划和实施管理评审时应考虑下列内容:
a)以往管理评审所采取措施的情况;
b)与质量管理体系相关的内外部因素的变化;
c)下列有关质量管理体系绩效和有效性的信息,包括其趋势:
1)顾客满意和有关相关方的反馈;
2)质量目标的实现程度;
3)过程绩效以及产品和服务的合格情况;
4)不合格及纠正措施;
5)监视和测量结果;
6)审核结果;
7)外部供方的绩效。
d)资源的充分性;
e)应对风险和机遇所采取措施的有效性(见 6.1);
f)改进的机会。
管理评审输出
管理评审的输出应包括与下列事项相关的决定和措施:
a)改进的机会;
b)质量管理体系所需的变更;
c)资源需求。
应保留质量管理评审会议的演示文稿、会议纪要和报告。
标准将于2019年7月1日实施。
点击“阅读原文”可下载










